Veselības Inspekcija (turpmāk - Inspekcija) informē uzņēmējus un patērētājus par medicīnisko termometru dokumentācijas, etiķetes un tirdzniecības iepakojuma novērtēšanas pasākumiem pirms termometru iegādes, lai pārliecinātos par preces kvalitāti un atbilstību medicīnisko ierīču prasībām.
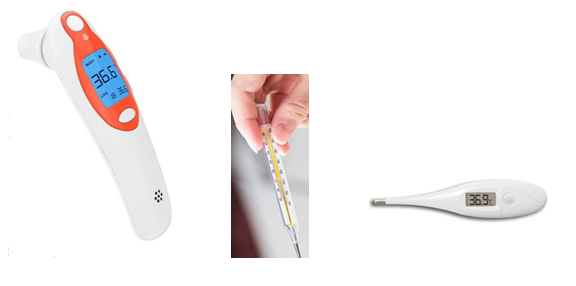
Par medicīniskām ierīcēm ir uzskatāmi dažāda veida termometri, kas paredzēti cilvēka ķermeņa temperatūras mērīšanai, t.sk.:
- digitālie termometri, kas paredzēti temperatūras mērīšanai zem mēles vai padusē;
- bezkontakta, infrasarkanā starojuma termometri u.c.
Termometriem, kas ir klasificējami kā medicīniskas ierīces, prasības noteiktas Ministru kabineta 2023.gada 15.augusta noteikumos Nr. 461 „Medicīnisko ierīču noteikumi” (turpmāk – Noteikumi Nr. 461) un Eiropas Parlamenta un Padomes Regulā (ES) 2017/745 (2017. gada 5. aprīlis), kas attiecas uz medicīniskām ierīcēm (turpmāk – Regula 2017/745).
Ņemot vērā, ka medicīniskie termometri tiek klasificēti gan kā I riska klases medicīniskas ierīces ar mērīšanas funkciju, gan kā IIa riska klases medicīniskas ierīces, papildus ražotāja sastādītai EK atbilstības deklarācijai nepieciešams paziņotās iestādes izdots apliecinājums par atbilstības novērtēšanas procedūras izpildi (EK sertifikāts).
Ja preces ražotājs atrodas ārpus Eiropas Savienības (ES), uz preces tirdzniecības iepakojuma un lietošanas instrukcijas jābūt norādītam ražotāja pilnvarotā ES pārstāvja nosaukumam un adresei.
Inspekcija vērš uzmanību uz sekojošiem pasākumiem, kurus ieteicams veikt pirms medicīniskā termometra iegādes.